|
| |||
|
Týdeník věnovaný aktualitám a novinkám z fyziky a astronomie. | |||
|
Překvapivá zpráva o vodě
AV ČR
Tisková zpráva AV ČR, 9. 5. 2007
Nejnovější vědecký objev, na němž se významně podílí tým z Akademie věd České republiky, publikoval v těchto dnech významný americký vědecký časopis.
Počítačové simulace, které se uskutečnily v Ústavu organické chemie a biochemie AV ČR v týmu doc. Pavla Jungwirtha ve spolupráci s kolegy na Hebrejské univerzitě v Jeruzalémě a na Univerzitě v Grenoblu ukazují, že monomolekulární povrchová vrstva čisté vody je ve skutečnosti kyselá s pHpH – záporně vzatý dekadický logaritmus koncentrace hydroxoniových iontů H3O+: pH = –log[c(H3O+)]. Chemicky čistá voda má pH = 7, kyseliny od 0 do 7, zásady od 7 do 14. v rozmezí 1,9 až 4,8.
|
pH – záporně vzatý dekadický logaritmus koncentrace hydroxoniových iontů H3O+: pH = –log[c(H3O+)]. Chemicky čistá voda má pH = 7, kyseliny od 0 do 7, zásady od 7 do 14. Aerosol – homogenní směs malých částic v plynu. Částice mohou být kapalné (mlha), nebo pevné (dým). Aerosoly se do atmosféry uvolňují jak přirozeně (během sopečné činnosti, požárů lesů), tak i působením člověka (spalováním fosilních paliv). Množství aerosolů v atmosféře má vliv na globální ochlazování (na aerosolech je rozptylováno sluneční světlo). Proteiny – bílkoviny, velké organické molekuly tvořené aminokyselinami uspořádanými do lineárních útvarů. Tyto dlouhé řetězce jsou pospojovány peptidovými vazbami (vazba karboxylové skupiny jedné molekuly a aminoskupiny druhé molekuly). |
Tento překvapivý teoretický výsledek publikoval prestižní vědecký časopis Proceedings of the National Academy of Science, USA. V článku se uvádí, že povrch čisté vody překvapivě není pH neutrální, ale kyselý (pH < 4,8). Týká se to horní monomolekulární vrstvy, což se neprojevuje kyselou chutí, ale tato skutečnost může zásadně ovlivnit řadu procesů od chemie atmosférických aerosolůAerosol – homogenní směs malých částic v plynu. Částice mohou být kapalné (mlha), nebo pevné (dým). Aerosoly se do atmosféry uvolňují jak přirozeně (během sopečné činnosti, požárů lesů), tak i působením člověka (spalováním fosilních paliv). Množství aerosolů v atmosféře má vliv na globální ochlazování (na aerosolech je rozptylováno sluneční světlo)., přes technologie, po acidobasické procesyAcidobasický proces – proces, kterého se zúčastní kyselé i zásadité látky. na povrchu proteinůProteiny – bílkoviny, velké organické molekuly tvořené aminokyselinami uspořádanými do lineárních útvarů. Tyto dlouhé řetězce jsou pospojovány peptidovými vazbami (vazba karboxylové skupiny jedné molekuly a aminoskupiny druhé molekuly)..

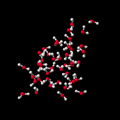
Typický záběr ze simulace vody metodou molekulární dynamiky. Zobrazen je povrchově vázaný hydroxoniový iont H3O+ (červenobíle) a objemově vázaný hydroxidový iont OH– (oranžovobíle). Modrobíle je znázorněna samotná vrstva vody. Zdroj: P. Jungwirth, Ústav organické chemie a biochemie AV ČR, v. v. i.
Schopnost vody se spontánně autoionizovat na hydroxoniové (H3O+) a hydroxidové (OH–) ionty je zcela zásadní pro technologické, atmosférické a biochemické procesy ve vodných roztocích. Nepřímo o tom víme, když si myjeme vlasy pH-neutrálním šamponem. Nejspíš ale nevíme, že pHpH – záporně vzatý dekadický logaritmus koncentrace hydroxoniových iontů H3O+: pH = –log[c(H3O+)]. Chemicky čistá voda má pH = 7, kyseliny od 0 do 7, zásady od 7 do 14. se na povrchové vrstvě vody může značně lišit od neutrální hodnoty 7.
Nový teoretický výsledek podporují i spektroskopická měření povrchů vody, vodných roztoků a ledových nanokrystalů, která se dělala na Oklahomské univerzitě a v dalších laboratořích ve Spojených státech amerických.
Současné výsledky ukazují, že molekulární povrch vody má neočekávané vlastnosti, které se mohou výrazně projevit v systémech s velkým poměrem povrchu k objemu. To může významně ovlivnit acidobasické procesyAcidobasický proces – proces, kterého se zúčastní kyselé i zásadité látky. na mikroskopických kapkách v atmosféře (aerosolech), ale také například na površích hydratovaných proteinůProteiny – bílkoviny, velké organické molekuly tvořené aminokyselinami uspořádanými do lineárních útvarů. Tyto dlouhé řetězce jsou pospojovány peptidovými vazbami (vazba karboxylové skupiny jedné molekuly a aminoskupiny druhé molekuly)..
Články o tomto objevu vyšly zároveň v britském Chemistry World a americkém Chemistry & Engineering News.
Klip týdne: Voda
Voda. V animaci si postupně na molekulární úrovni prohlédnete vodu vázanou ve formě ledu, poté ve formě chladné kapky a na závěr ve formě horké kapky, ze které se odpařují jednotlivé molekuly do okolí. Zdroj: Chamot Laboratories, Inc. (gif, 1,6 MB)
Odkazy
Tisková zpráva AV ČR z 9. 5. 2007
Victoria Buch et al.: Water Surface is Acidic, text of the paper, 2007